Um estudo realizado por membros do Laboratório de Bioquímica de Complexos Bacterianos da Universidade Estadual de Campinas (LaBiCoBac/UNICAMP), em colaboração com o Instituto Europeu de Química e Biologia, revelou detalhes importantes sobre um dos mecanismos pelos quais bactérias podem adquirir novos genes, como aqueles responsáveis pela resistência a antibióticos. A pesquisa, publicada no EMBO Journal hoje (18 de outubro), concentrou-se em compreender o funcionamento, a nível molecular, de algumas das peças-chave desse processo e resultou em descobertas que podem ser essenciais para o desenvolvimento de novos medicamentos para tratar infecções bacterianas em animais e plantas.
Em busca de se aprofundar no mecanismo de transformação natural bacteriana — o processo pelo qual uma bactéria captura DNA de fora da célula e o incorpora em seu próprio genoma — a equipe de pesquisadores focou as análises em duas enzimas reconhecidas por sua participação ativa nesse processo, a RadA e a ComM. Além de purificar e estudar essas proteínas utilizando a crio-microscopia eletrônica (CryoEM), uma técnica avançada de microscopia em que as amostras são analisadas congeladas, também conduziu ensaios bioquímicos que auxiliaram na compreensão da dinâmica e da atividade dessas estruturas durante a transformação.
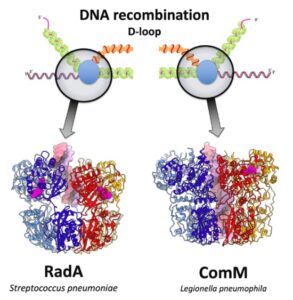
Entre as descobertas, destacam-se a semelhança estrutural da dupla, bem como uma inesperada similaridade na forma com que ambas convertem energia química durante sua atividade biológica — aumentar a região que sofrerá troca de informações genéticas. Por outro lado, foram observadas diferenças significativas na maneira como utilizam essa energia, assim como no desempenho e na organização do DNA em que estão ligadas. Enquanto a RadA parece ter maior eficiência na separação das fitas de DNA e um papel primário na reestruturação dessas regiões, a ComM mostra-se mais relevante durante a translocação do DNA, ou seja, no movimento ou transporte ao longo de segmentos de material genético dentro da célula e durante processos como a recombinação genética, aponta o artigo.
Leonardo Talachia Rosa, pesquisador da UNICAMP e autor do estudo, explica que ambas as enzimas estudadas são fundamentais para a evolução desses organismos no contexto da infecção. “As helicases caracterizadas participam de um processo muito importante denominado de transformação natural, onde as bactérias incorporam material genético exógeno em seus genomas através de troca de fitas de DNA”, relata o autor. “Esse processo leva a possibilidade da aquisição de novos genes de virulência, genes de resistência a antibióticos, formas de evasão do sistema imune, entre outros”, complementa, elucidando como os avanços da pesquisa podem ser essenciais para entender processos de alta relevância em contextos de biotecnologia e saúde, por exemplo.
Embora o objetivo do estudo seja a elucidação, a nível molecular, de como as helicases RadA e ComM atuam, no futuro, os dados podem servir como base para modificações intencionais nos processos conduzidos por elas, o que pode contribuir para o desenvolvimento de novas formas de tratamento de infecções causadas por bactérias. “Os resultados podem iluminar o caminho para o desenho de novos fármacos que ataquem diretamente essas helicases e reduzam a capacidade adaptativa dessas bactérias no contexto da infecção”, conclui o pesquisador.
O LaBiCoBac integra atualmente o Centro de Pesquisa em Biologia de Bactérias e Bacteriófagos (CEPID B3).

